
11/2020
一、单晶培养与结构解析
主要通过溶液法,包括溶剂缓慢挥发、变温、液\气相扩散、界面法等,获得化合物符合测试条件的单晶样品,并进行单晶结构数据的收集和解析。晶体结构可用于确认化合物的分子绝对构型、分子堆砌规则和分子间相互作用。

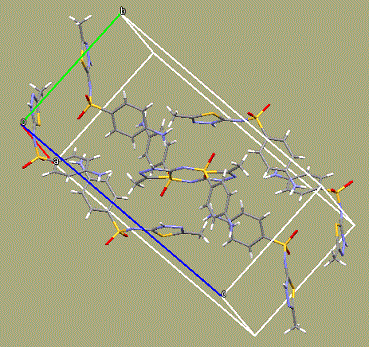
二、药物共晶虚拟筛选
药物多晶型、盐型和共晶可拥有不同的理化性能,药物开发要对这些固体形态进行筛选,获得优选的形式进行后续开发。我们提供特色的共晶虚拟筛选方案,确认候选小分子中哪些与药物形成共晶的可能性更大,以减少实验工作量。

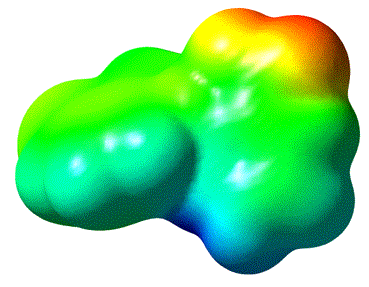
三、固体核磁共振
提供药物晶体学领域固体核磁共振解决方案。包括晶相指纹谱、晶型定性定量分析、离子状态判定(是否成盐)、制剂中活性组分晶型探测、无定型分散物互混状态分析等。

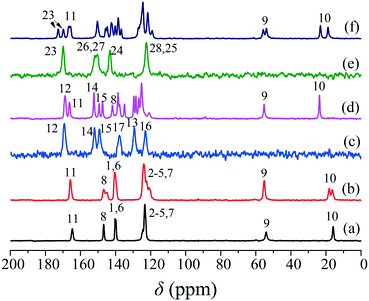
四、DSC分析
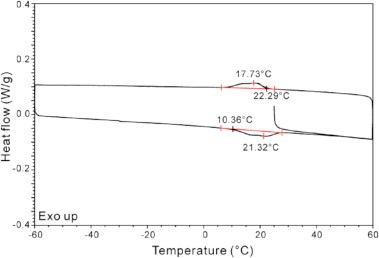
对晶型及无定型体系进行热力学分析,获取熔点、相转化及相关焓值信息,判定不同晶型的热力学互变关系。设备包括先进的调制DSC模式,可区分可逆与不可逆热流信息。

项目联系人:张老师,邮箱:hlzhang2008@sinano.ac.cn
11/2020
人类microRNA表达谱检测
microRNA(miRNA)是一类长度约为22 nt的非编码小RNA,在转录后水平调控基因的表达。大量研究表明,miRNA几乎参与所有的生命活动,与动植物生长发育、抗逆胁迫,以及人类疾病的发生紧密相关,已成为基础生物学、医学、临床诊断等研究领域的热点。
本平台采用的非标记miRNA芯片UnitagTM可高通量筛选不同样本中差异表达的miRNA,该芯片与其他芯片和测序技术相比,不仅检测性能(特异性、灵敏度)一致,且无需对样本进行标记和酶反应,大幅减少多步骤反应带来的实验误差,提高检测结果的真实性,同时降低了检测成本。
具有上述优势的miRNA非标记芯片,我们可提供人类miRBase 19.0版本的miRNA表达谱检测。
UnitagTM microRNA芯片技术特点
1, 微阵列使用独特的堆积杂交通用探针技术,可直接使用总RNA进行检测。
2, 无需分离纯化小RNA。
3, 无需对样品进行任何形式的标记处理,最大限度确保小RNA分子的完整性。
4, 从根本上排除了化学标记过程中由于碱基选择基因的测量偏倚(bias)。
5, 检测过程100%不使用酶,完全避免了酶反应过程引入的标记和杂交效率差异。
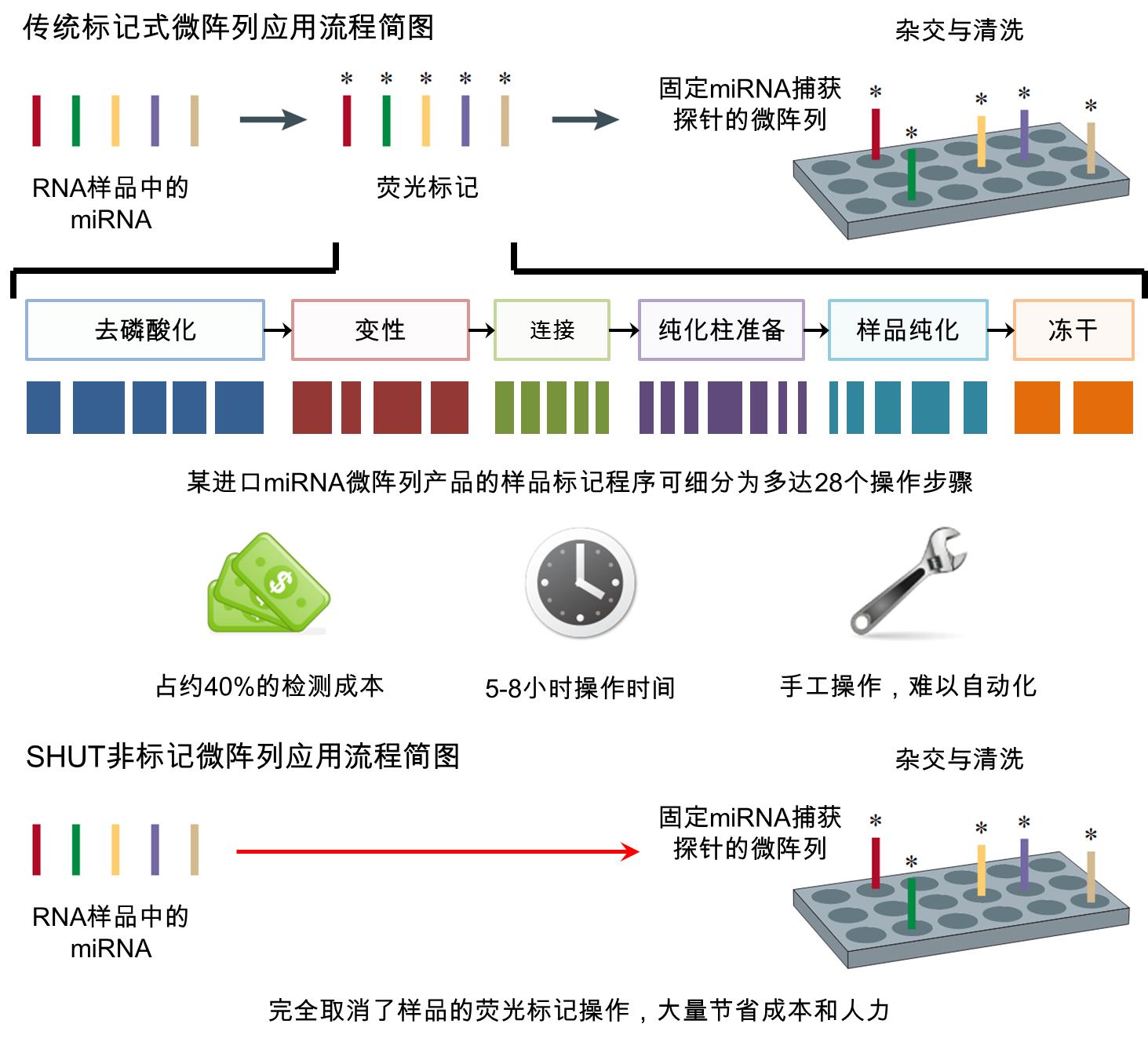
UnitagTM microRNA芯片性能指标
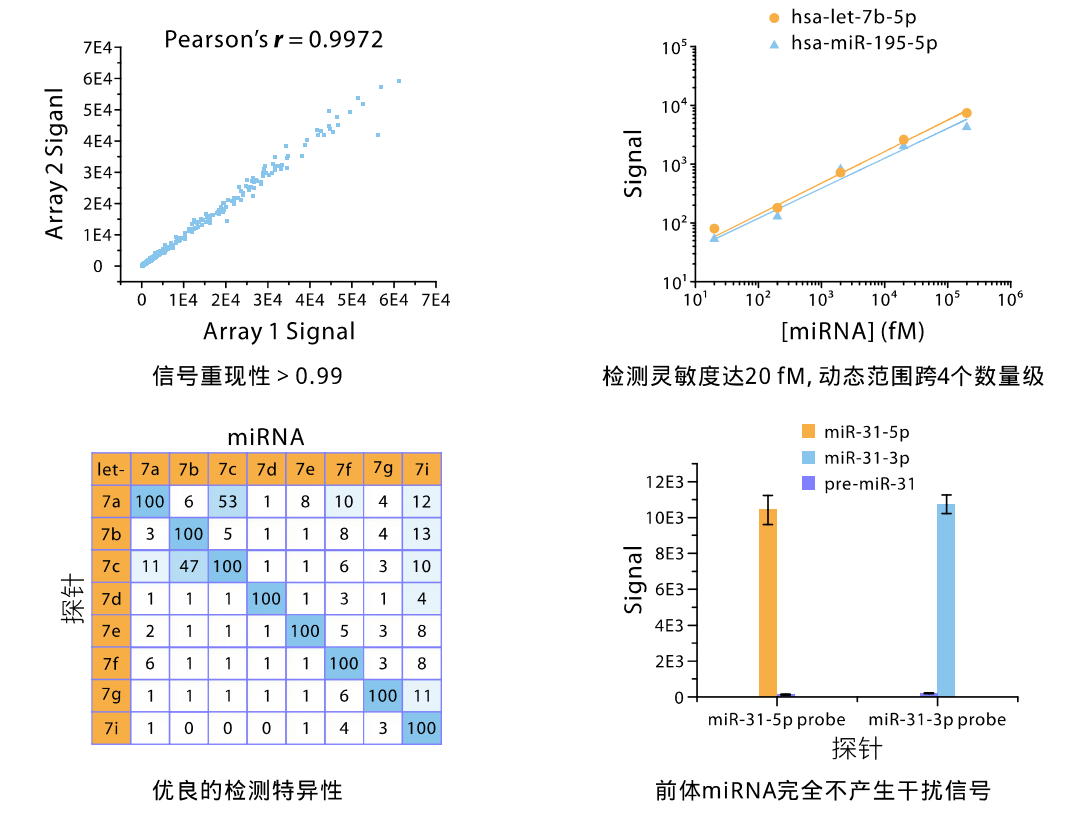
UnitagTM microRNA芯片客户数据示例
1, 差异表达miRNA的聚类图
聚类分析是通过数据建模简化数据的一种方法,目的在于获得数据的分布状况,观察每一簇数据的特征。绿色色阶标示了下调表达的基因,红色色阶标示了上调表达的基因。
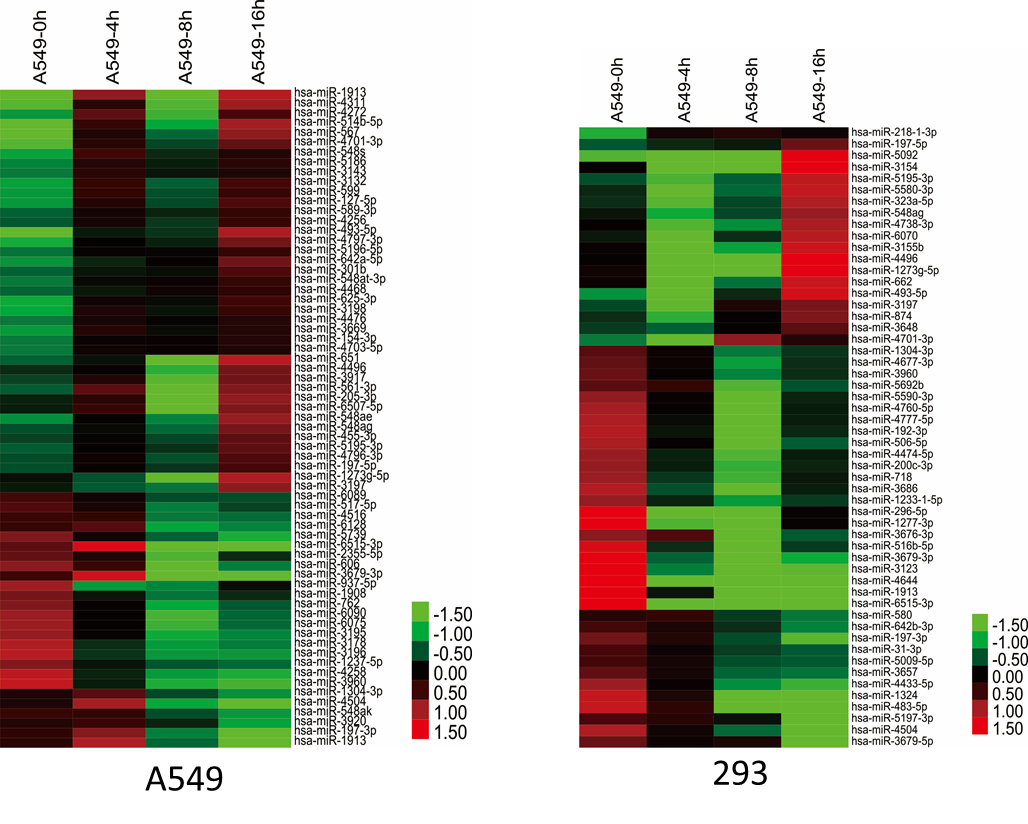
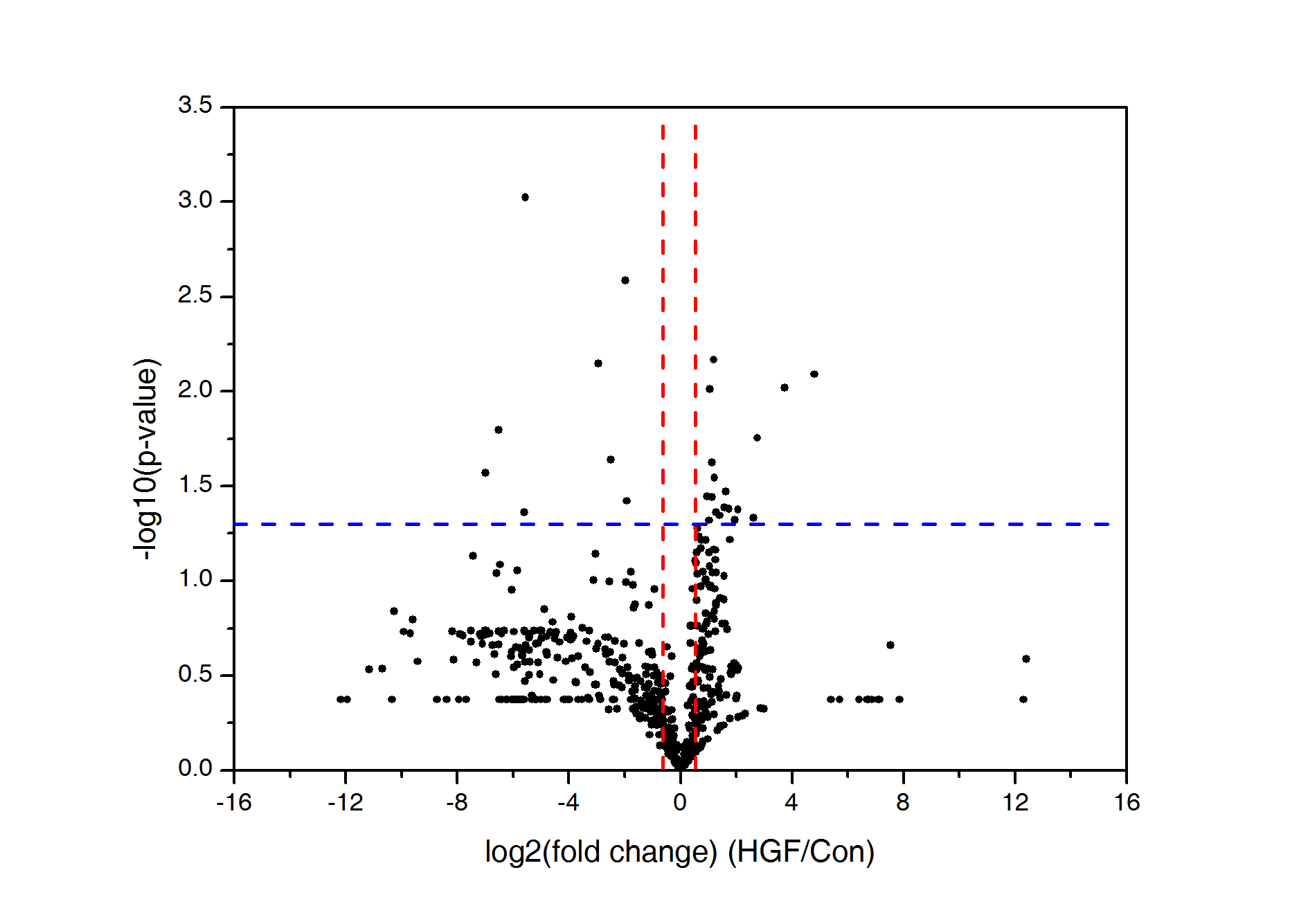
2, 差异表达miRNA的火山图
火山图可以对不同样品组之间差异表达的miRNA进行图形化的展示。横轴代表处理组和对照组之间miRNA表达倍数的变化(log2转化),纵轴代表相应的p值(-log10)转化。火山图可以直观展示miRNA在样品组间的倍数变化与相应的统计学显著性之间的关系。
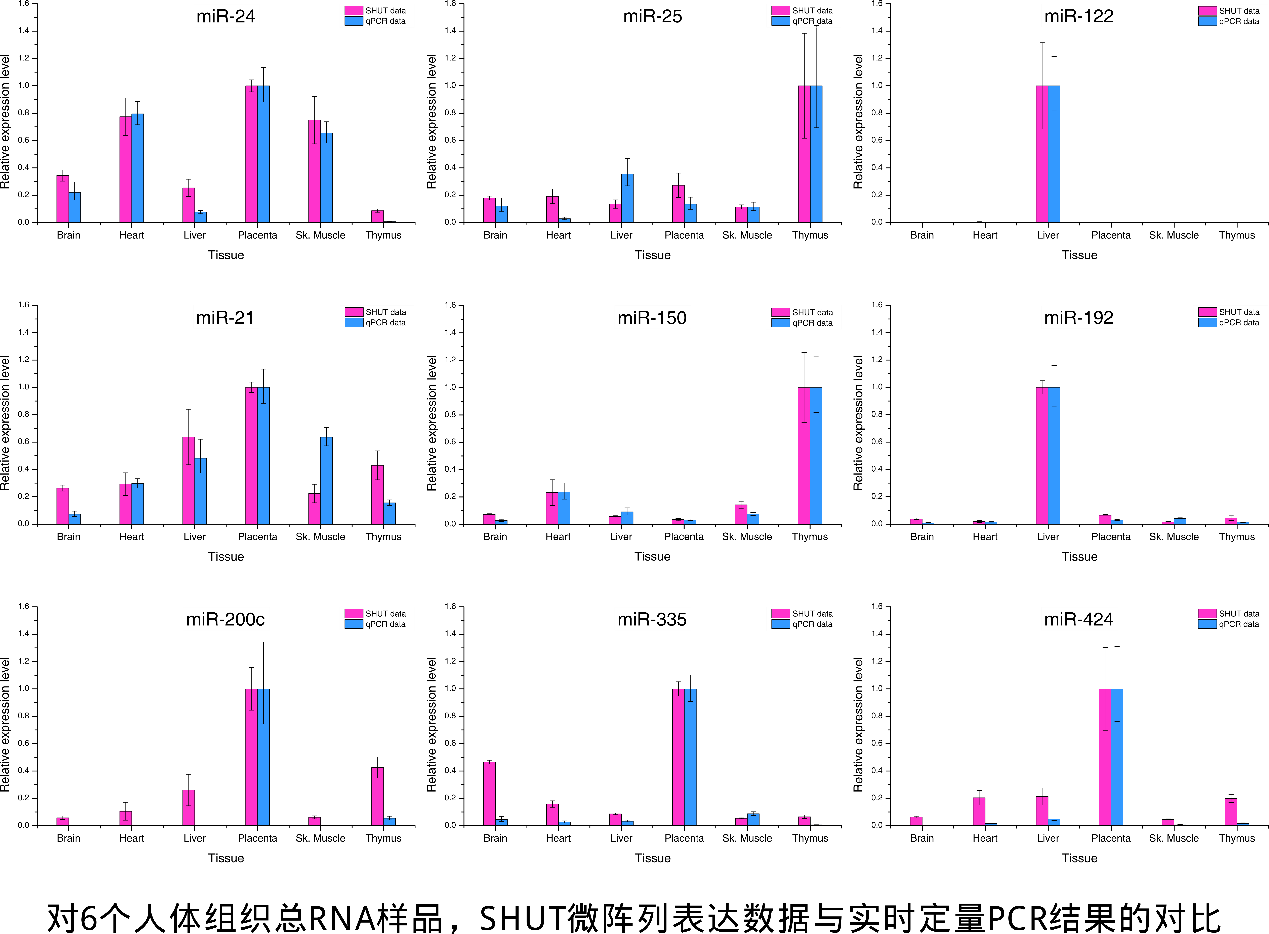
3, 差异表达miRNA的实时定量PCR验证
实时定量PCR(qPCR)是验证芯片表达的“金标准”。通过高通量芯片筛选出的差异表达miRNA,采用qPCR实验方法其进行验证,为下游实验的开展提供保障。下图为6种人体组织中,UnitagTM miRNA芯片数据与qPCR结果的对比。
芯片类服务联系人:沈叶 0512-62872643 yshen2010@sinano.ac.cn
11/2020
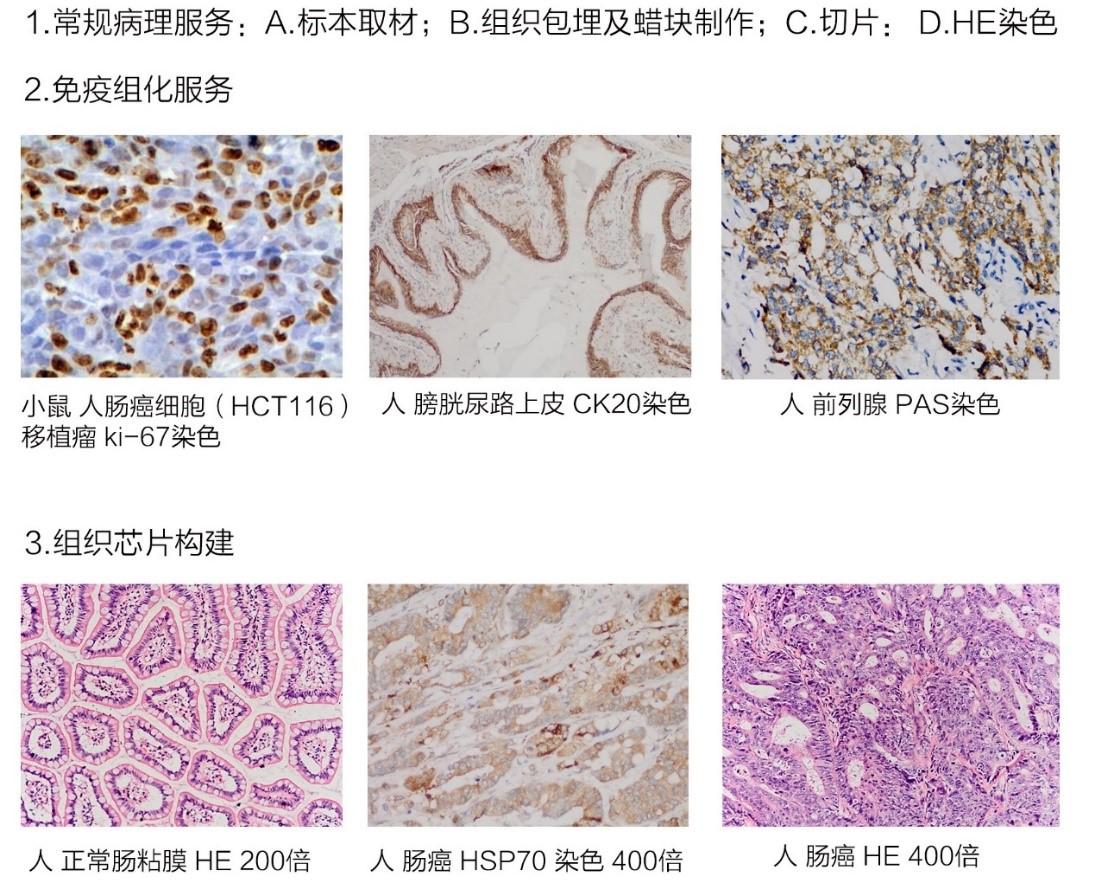
组织切片从生物组织取材,处理为薄片,染以颜色,以期保留组织的最真实状态,应用玻片以合适的显微镜观察,用以直接判定组织最真实情况,为后期进治疗或实验提供指导性意义。纳米生化平台现推出病理组织相关服务,为您提供专业、快速及可靠的病理分析服务,主要包括临床样本病理诊断结果复核,免疫组化结果判读,肿瘤学及毒理学动物模型病理表型分析以及投稿前病理图片审核等。同时可以提供包括镜下病理描述、数码图片及实验结果分析在内的专业病理分析报告。我们的病理技术服务平台,涵盖了从实验标本取材,蜡块制作、切片染色(HE及各项特殊染色)至免疫组化服务及组织芯片构建等各个层面。
免疫组化技术平台拥有多种经过预实验验证的抗体,建立了相应的实验方法,极大的提高了实验结果的可靠性,免去抗体订购等实验流程,缩短实验周期,降低实验投入;组织芯片构建平台采用进口预制蜡块,多种通量可供选择,点阵排列整齐,黏附性极佳,构建过程快速高效。


赛默飞Histocentre 3 包埋机


莱卡RM2235切片机


莱卡ASP300脱水机


莱卡autostainer xl染色机
我们的优势:
1, 多年的动物病理切片的判读能力,能够准确判读病理变化。例如免疫组化判读需要准确判断抗体定位和强弱,目前存在最常见问题是往往一些非特异性染色,在研究人员眼中会被判读成细胞浆阳性,染色强弱评分需要有专业经验。甚至有一些所谓判读的结果,肿瘤的位置未能准确找到,把正常组织误以为是肿瘤。
2, 准确的病理形态描叙。
3,我们的组织芯片有以下优点:受体蜡块采用预制蜡块非手工排点,点阵排列整齐;特质专利受体蜡块配方,熔蜡效果好,结合紧密,与不同供体蜡块兼容度高;
4,组织芯片制作中,由专业病理研究院选取供体蜡块上代表性组织。
我们提供的服务:
一、病理分析服务(从收到样本起7个工作日出具分析报告):
1,病理切片复核(结果仅供科研用途)
2,免疫组化结果判读(结果仅供科研用途)
3,动物模型病理表型分析:
A,肿瘤学模型;B,毒理学模型
4,稿件病理图片审核
5,数码图像采集
6,病理切片扫描
二、病理技术服务:
实际例证:
小鼠毒理模型病理结果分析
材料方法:小鼠心、肝、脾、肺及肾脏制作HE切片,观察各组之间各脏器组织结构及细胞形态的差别。
组别及命名原则:
本次实验共分为5组:P22(PEI)、P22(MAL)、阿(游离)、阿(脂)、PBS。
组别+脏器名称缩写。H:心脏,Li:肝脏,S:脾脏,Lu:肺脏,K:肾脏。
镜下所见:(代表性数码照片见附件)
心脏:形态正常
描述(适用于所有小鼠):心肌细胞胞浆丰富,横纹清晰;细胞核居中,核膜正常,核形态规则,为卵圆形,染色质致密或成空泡样。
肝脏:
描述:P22(MAL)、阿(脂)及PBS组:肝小叶结构清晰可见,肝板结构存在,肝细胞单层排列,大小正常,胞浆粉染,核规则,肝窦存在。
P22(PEI)及阿(游离)组小鼠肝脏形态大致正常,部分区个别肝细胞细胞核增大(肝细胞出现双核很正常,肝板之间出现裂隙是由于固定脱水肝组织收缩造成的人工现象,不是肝脏畏缩的表现),间质内炎症细胞浸润,周围血管扩张、淤血。
脾脏:形态正常
描述(适用于所有小鼠):脾脏结构清晰,红髓及白髓比例正常,灶区脾窦扩张,轻度淤血(脾脏为小鼠体内最大的储血器官,脾窦内有红细胞聚集为正常表现);红髓内出现巨核细胞,表示有髓外造血表现。
肺:形态正常
描述(适用于所有小鼠):肺泡结构清晰,肺泡上皮细胞无异型,肺泡间隔正常,个别肺泡腔轻度扩张(灶区小支气管上皮出现鳞状化生,生理性现象,不是毒理学表现)。
肾脏:形态正常
描述(适用于所有小鼠):肾脏皮质及髓质比例正常,皮质内肾小球结构清晰,包氏囊存在,未见明显系膜细胞增生。皮质及髓质内近远端肾小管管腔开放,未见管型,肾盂被覆正常尿路上皮。(肾小管上皮轻度水肿,胞浆稍丰富,胞界不清,未构成明显的毒理学改变)
结论:
本毒理模型中,模型中心,脾,肺及肾脏保持正常组织学结构及细胞形态,未见明确病理性改变,也未见明确毒理学特征。肝脏见轻微炎症性改变,可能由药物毒性引发。
| 服务 | 类别 | 价格(RMB) | |
| 综合 | 取材+蜡块+切片+染色+判读 | 一个蜡块+5张白片 | 160元/例 |
| 取材+蜡块+切片+免疫组化+判读 | 一个蜡块+5张白片 | 240元/例 | |
| 病理分析服务 | 病理切片复核 | <50例 | 65元/例 |
| >50例 | 50元/例 | ||
| 免疫组化结果判读 | <50例 | 40元/例 | |
| >50例 | 35元/例 | ||
| 组织芯片免疫组化结果判读 | <500点 | 15元/例 | |
| >500点 | 12元/例 | ||
| 动物模型病理表型分析 | <50例 | 65元/例 | |
| >100例 | 50元/例 | ||
| 稿件病理图片审核 | - | 1500元/次 | |
| 数码图像采集 | - | 12元/张 | |
| 病理切片扫描 | - | 65元/张 | |
| 病理技术服务 | 标本取材 | 小标本 | 8元/例 |
| 大标本 | 150元/例 | ||
| 组织包埋及蜡块制作 | <300例 | 25元/例 | |
| >300 | 20元/例 | ||
| 常规切片 | <500张 | 15元/张 | |
| >500张 | 12元/张 | ||
| 冰冻切片 | 240元/张 | ||
| 染色 | <500张 | 15元/张 | |
| >500张 | 12元/张 | ||
| 免疫组化服务 | 普通切片 | 200元/张 | |
| 组织芯片 | 450元/张 | ||
| 组织芯片构建 | 预制蜡块 | 800元/块 | |
| 构建费 | 30元/点 | ||
| 切片费 | 30/张 |
联系人:郑克孝 kxzheng2007@sinano.ac.cn 秦静怡 jyqin2014@sinano.ac.cn 0512-62872644
11/2020
Biacore T200代表了Biacore产品家族的最新研发成果,它具有最高的灵敏度和最低的噪音,在仪器的灵敏度和应用的多样性方面有了显著的改善。
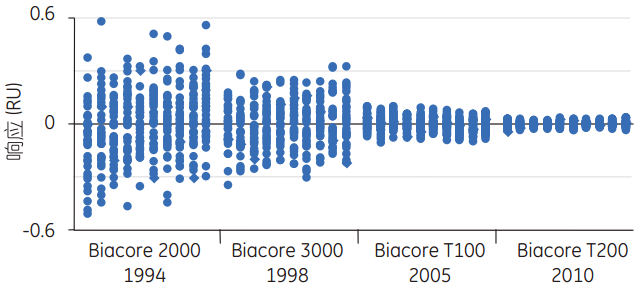
图1 Biacore仪器的短期噪音比较
(一)T200技术参数
技术项目 | 参数 |
检测原理 | 表面等离子共振原理(SPR) |
获取的信息 | 动力学、亲和力、特异性、活性浓度、热力学等 |
样品类型 | 从低分子量化合物到生物大分子如蛋白、多肽、DNA、RNA、多糖、脂类分子以及细胞及病毒,含DMSO等有机溶剂的缓冲液,血清及胞浆上清液等 |
结合速率常数(ka) | 103-3X109 M-1S-1 |
解离速率常数(kd) | 10-5-1 S-1 |
平衡常数(KD) | 10-4-3.3X10-15 M |
分析温度 | 4-45℃ |
分子量下限 | 对有机化合物无分子量限制 |
样品折射率范围 | 1.33-1.40 |
动态范围 | 1-70000 |
基线噪音 | < 0.03 RU (RMS) |
浓度测定 | 标准曲线法或CFCA法 |
(二)T200性能表现
一、扩展非标记相互作用分析的检测极限
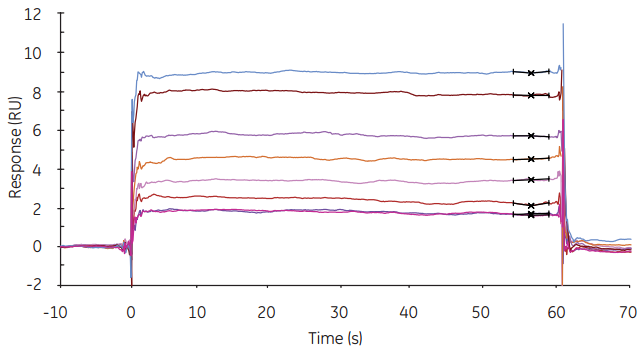
图2 甲基磺酸(Mr 95)与碳酸酐酶的相互作用特性
Biacore T200专为要求高灵敏度的分子间相互作用的分析而设计:
1)小的有机化合物(无最低分子量限制)
2)低丰度分子(浓度大于10pM)
3)稀有或敏感的靶蛋白,如G蛋白偶联受体
4)避免了分析与二价抗体之间相互作用时亲和效应的干扰
5)微弱相互作用分析,KD在mM范围内
6)稳定的结合物,kd≥10-5 S-1
1、测定稀有或敏感靶蛋白
从低水平捕获蛋白获取高质量数据有利于分析小分子和诸如G蛋白偶联受体等敏感蛋白的相互作用,而这些蛋白往往是最重要的药物靶蛋白。而Biacore T200的高灵敏性意味着蛋白固定后仅需小部分分子保留活性即可用于分析。此外,稀有靶蛋白使用量较少,使得消耗降低的同时并不影响数据质量。敏感靶蛋白的研究因此更加可信,缩短了药物发现过程中的检测时间。
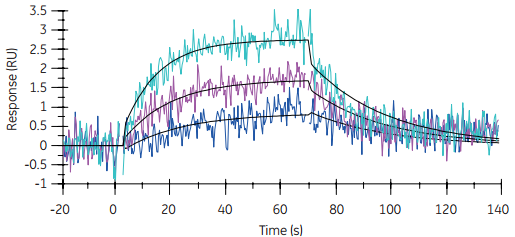
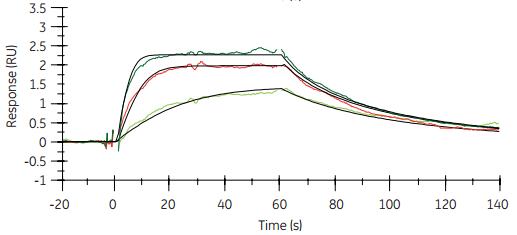
图3 小分子黄嘌呤胺同源物(XAC)与组氨酸标记GPCR(STaRR)A2的结合。当使用低水平固定GPCR时,采用Biacore T200(右图)可生产质量优于Biacore T100(左图)的数据。
2、分析方法设计更加灵活
在评估抗体用作治疗、分析或诊断工具的适用性时,对抗原-抗体相互作用进行全面特征鉴定很重要。当利用Biacore进行抗原-抗体分析时,通常情况下建议将抗体固定于传感器表面以免其亲和作用(Avdity Effect)影响数据解读。然而,在特定情况下,人们更倾向于固定抗原,这是出于节约珍贵靶分子的考虑或抗原分子更易于固定。Biacore T200的高灵敏度足以降低抗原捕获水平以避免亲和效应,进而使得分析方法的设计可以灵活多样。
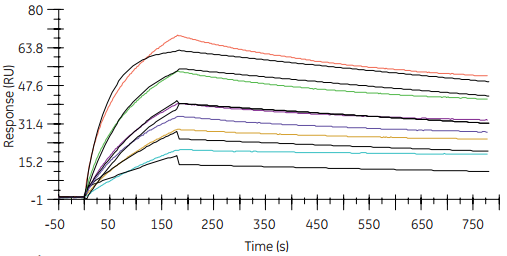
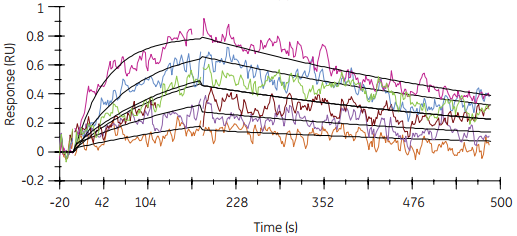
图4 在抗原低捕获水平上(右图)分子间相互作用数据更适合1:1模型。从而以抗体为配体的相应动力学常数的计算更加精确、可靠。
3、更广动力学范围内的高度精确性分析
Biacore T200中的微流控系统经过优化以用于高质量的动力学分析。四个流动池可灵活用于单一的、配对的或者系列运行。配对的芯片上流动池接口使得流动池之间的空间被降到最低水平,确保了精确的标准差减。
Biacore T200可以测定从最快的结合速率到最慢的解离速率的最广范围内的动力学常数。这可用于对强结合物进行排序,这一点对于抗体筛选非常重要。此外还可以用于检测快速结合的相互作用物之间的差别,这在收到生物利用率限制的生物学过程的研究中非常重要。
1)ka从103到5X107M-1s-1(对于大分子待检物为103到3X109 M-1s-1)
2)kd从10-5到1s-1
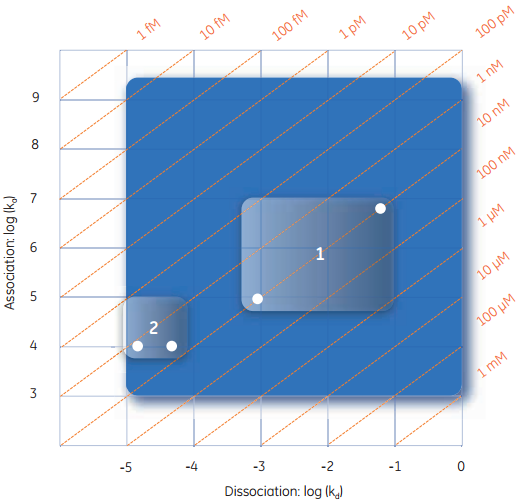
图5 从最快结合速率到最慢解离速率的最大范围内动力学参数测量。具有明显类似亲和力的相互作用具有极其不同的动力学特性。
二、性能范围
1、自动运行条件下可分析高达384种样品
Biacore T200支持96和384孔板和小瓶的使用。四个流动池的使用使得四种相互作用可被同时检测。Biacore T200的样品槽可以降温到4℃,使得敏感样品可以在高达48小时无人值守的运行中得以分析。
2、在生理温度下研究分子间相互作用来预测体内状态的情况
通过提高在生理温度下测定的可靠数据,Biacore T200确保更加准确地预测体内状态下的治疗性分子的特性。系统一体的缓冲液除气装置防止在温度升高的情况下形成气泡,有助于确保更高质量的数据。此外,一体的除气装置也可以省略运行前对缓冲液进行的除气操作。
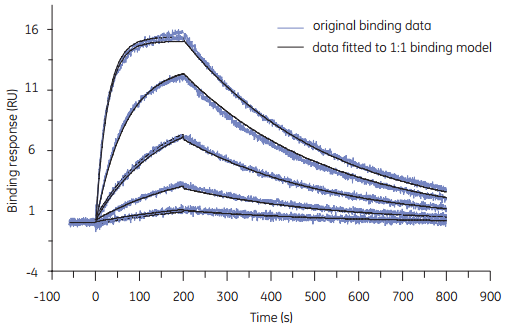
图6 Biacore T200在37℃时提供稳定和可重复的数据。
3、运行缓冲液筛选有助于快速分析方法开发
内置的缓冲液选择装置在每次运行中可最多测试四种缓冲液,加快了分析方法的开发。例如,结合特性的微环境效应可在机制性和稳定性研究中进行分析。
4、回收样品以用于质谱鉴定
Biacore T200结合质谱为在功能性结合标准的基础上鉴定蛋白质提供了可能。样品的回收及消化均具有软件支持。
1)被分析物以很小的体积被回收,使得浓度最大化。
2)从样品到回收溶液尽可能减少残留。
3)在含有消化溶液的瓶中沉淀。
4)软件模板预先设置有整个回收过程。
三、快速、简单的动力学分析
Biacore T200软件为可信的和准确的动力学分析上提供了广泛的工具。可使用多循环方法;或者采用单循环动力学分析:由于不需要进行每次注入样品之间的表面再生过程,单循环动力学分析使得那些涉及难以再生的靶蛋白分析能够实现,并且缩短了分析开发的时间。
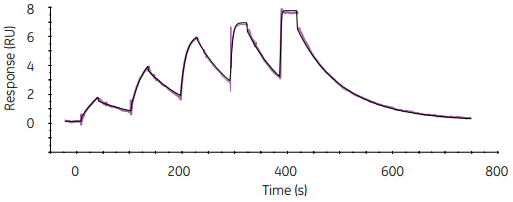
图7 使用单循环动力学分析方法,样品在无需中间再生步骤的情况下逐个被加入到同一个循环中。
Biacore T200数据评估软件可使分子间相互作用的动力学分析通过几个简单的点击来实现。
1)同时处理多重样品以简化数据分析过程并且节省时间
2)使用一个或几个现有的相互作用模型拟合动力学数据
3)自动减去参照和空白对照数据
(三)经典应用
1、绘制凋亡信号通路
通过研究点突变凋亡蛋白和细胞表面受体之间的相互作用可以揭示出细胞内的信号传导通路。
研究表明,凋亡蛋白LIGHT可与两种细胞受体:淋巴细胞毒素-β受体(LTβR)和疱疹病毒穿入介质(HveA)相结合。通过在可能参与受体结合的肽环处引入点突变,Biacore方法可考查这些突变对LIGHT蛋白结合特性的影响。
实验对野生型和LIGHT突变体与其受体间的相互作用分别进行了研究。通过抗体捕获技术讲HveA蛋白和LTβR蛋白固定于传感芯片表面。体外分析发现,其中一种LIGHT突变体可以与HveA蛋白结合,却不能与LTβR蛋白相结合,也没能导致靶细胞的凋亡。这些结果有力的暗示,LIGHT通过与其细胞表面受体相互作用时至少激活了两条不同的信号通路,而且只有其中一条通路会引发凋亡。
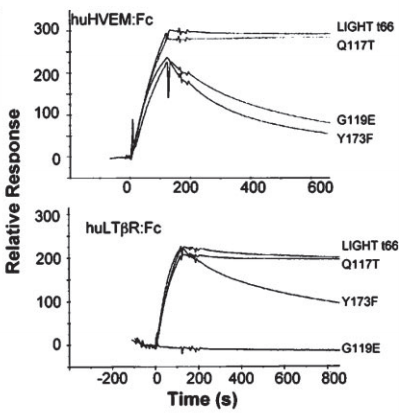
图8 LIGHTt66蛋白突变体Q117T与HveA蛋白结合(上),而不与LTβR蛋白结合(下)。
Reference: Rooney, I. A. et al. The lymphotoxin-β receptor is necessary and sufficient for LIGHT-mediated apoptosis of tumor cells. J. Biol. Chem. 275, 14307–14315 (2000)
2、配体垂钓
从细胞条件培养基中鉴定与细胞表面受体相互作用的可能配体。
将一个含细胞表面受体Flt4胞外域的Fc融合蛋白固定在传感芯片表面。将来自100种不同细胞系的浓缩培养基流经芯片表面。当把这些培养基用生物学方法检测时,只有在Biacore实验中能与Flt4结合的培养基才能够诱导稳定转染的CHO细胞中的Flt4受体发生酪氨酸磷酸化。
随后,经过亲和层析柱的分离和SDS-PAGE电泳,三种与Flt4结合活性相关的多肽被收集。
由收集到的其中两种肽段中部分氨基酸序列合成变性PCR引物,扩增出一个65 bp的产物。测序结果显示,该产物中含有一段和已知氨基酸序列完全匹配的序列。这段cDNA被用来鉴定Flt4的配体,确认该蛋白在新转染细胞中的生物功能,同时还可以用于发现与其功能相关的生长因子的同源区域,从而研究这些配体的基因表达状态。
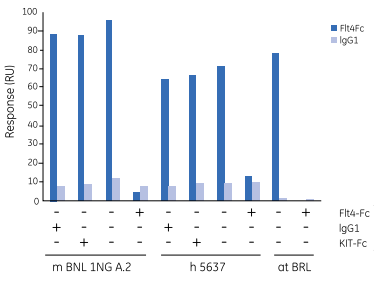
图9 与Flt4-Fc特异结合的三种细胞条件培养基(CM)。当CM与过量的Flt4-Fc(非人IgG-Fc)共注射时,该信号被抑制。
Reference: Fitz, L. J. et al. Characterization of murine Flt4 ligand/VEGF-C. Oncogene 15, 613–618 (1997)
3、蛋白-蛋白相互作用
研究多组分蛋白复合体对生物过程的调节
补体旁路(alternative complement)蛋白C3b部分受到血浆蛋白因子H(fH)的调节。通过对fH与表面结合蛋白C3b相互作用位点进行鉴定,有助于理解补体旁路为什么只会被异己组织激活。
将C3b连同其蛋白水解片段C3c和C3d固定于芯片表面。 将8个fH片段通过注射流经芯片表面,结果发现血浆蛋白因子H (fH) 上存在三种不同的与C3b结合的位点。
每个fH片段都与C3b上不同的位点相互作用。位点1仅与完整的C3b作用,位点2与C3b和C3c结合,而位点3与完整C3b和C3d片段结合。C3b和fH之间的多重交互作用对于理解补体旁路与异体和宿主结构之间存在的专一反应性提供了分子基础。
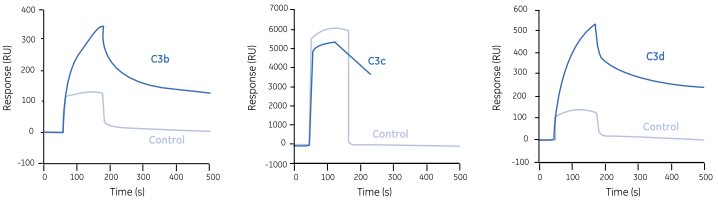
图10 fH位点3仅与完整C3b和其片段C3d相结合
Reference: Jokiranta, T. S. et al. Each of the three binding sites on complement factor H interacts with a distinct site on C3b. J. Biol. Chem. 275, 27657–27662 (2000)
4、Biacore系统与质谱
Biacore系统与电喷雾串联质谱技术(ESI-MS/MS)联合为研究者提供一种新的分析方法,用来捕获发生相互作用的蛋白并进行回收与鉴定。该技术提供了一整套包含检测、捕获及回收中低飞摩尔量级蛋白的方法。
将三磷酸肌醇(IP3)固定在芯片表面,将转化有IP3结合蛋白的细菌裂解物流经芯片表面。随后,通过空气隔断的方法(air partition method)将微量的胰酶送至结合蛋白处进行消化。酶解的肽段通过反相毛细管柱富集并除去了可能干扰质谱分析的杂质。从反相上洗脱的肽段混合物通过液质联用串联质谱系统进行分析,最终确定IP3结合蛋白的存在。
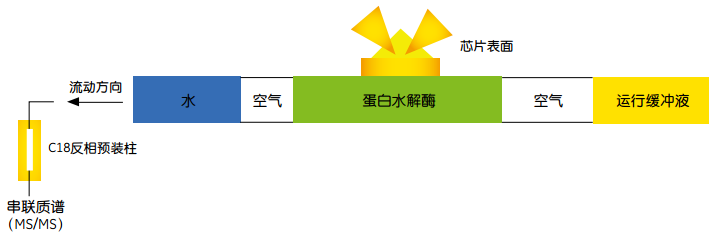
图11 表面在位消化原理。与芯片表面结合的蛋白质经蛋白酶原味消化和毛细管柱富集后进行串联质谱MS/MS分析。
Reference: Natsume, T. et al. Combination of biomolecular interaction analysis and mass spectrometric amino acid sequencing. Anal. Chem. 72, 4193–4198 (2000)
5、检测临床实验中治疗抗体的免疫源性
作为治疗药物,小鼠抗体由于会激起机体免疫应答而受到限制。纽约Ludwig肿瘤研究中心的研究人员构建出一个人源化的小鼠单克隆抗体药物,该药物将CDR区域嫁接进人IgG骨架,能识别人结肠上皮和结肠癌中特异表达的一种标记物。这种嵌合抗体在患有结肠癌的病人身上进行I期和II期临床检测,其免疫源性通过无标记蛋白相互作用分析进行监控。
将人源化抗体(huAb A33)固定在传感芯片表面,并在制备好的芯片表面注入病人的血清。反应人群被大体划分为两大类。 I型反应人群的特点是在2周时间内血清中出现有抗huAb A33的抗体,尽管病人持续接受huAb A33治疗,但抗huAb A33抗体的滴度开始不断下降。而另一边,II型反应人群的免疫应答反应较缓慢,但随着治疗的继续,抗体滴度持续增加。在后一组中,生理性不良反应比I型更加频繁,因此,最终停止了使用huAb A33对这些病人进行治疗。
此外,病人抗体响应的亚类也可通过Biacore夹心检测进行鉴定。简言;所有病人样品当预先将蛋白G加入稀释血清后(去除IgG)其抗huAb A33反应几近消失,而有一些病人采用正辛酸处理(沉淀所有的非IgG蛋白)则没有太大的影响。极少的病人在用蛋白G处理血清后仍有残留的活性存在,这些信号可通过向传感芯片表面注入抗IgM抗体检测到。
具有II型反应的病人数周内都没有出现不良生理症状,直到几周后,用Biacore检测到抗huAb A33抗体水平持续增加。因此研究人员可以采用无标记蛋白相互作用分析对可能出现的不良反应进行预测。
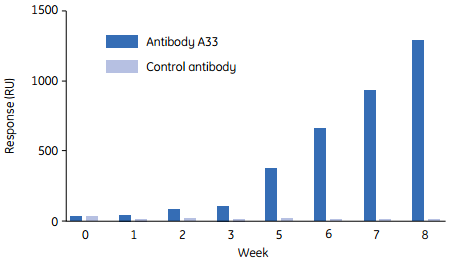
图12 II型病人体内人源化抗体的应答水平与单个病人所发生的临床免疫化学参数改变和不良反应之间的关联。
Reference: Ritter, G. et al. Serological analysis of human anti-human antibody responses in colon cancer patients treated with repeated doses of humanized monoclonal antibody A33. Cancer Res. 61, 6851-6859 (2001)
(四)实际案例
1、蛋白-蛋白相互作用
配体:蛋白HSA
分析物:蛋白HE,~6KDa
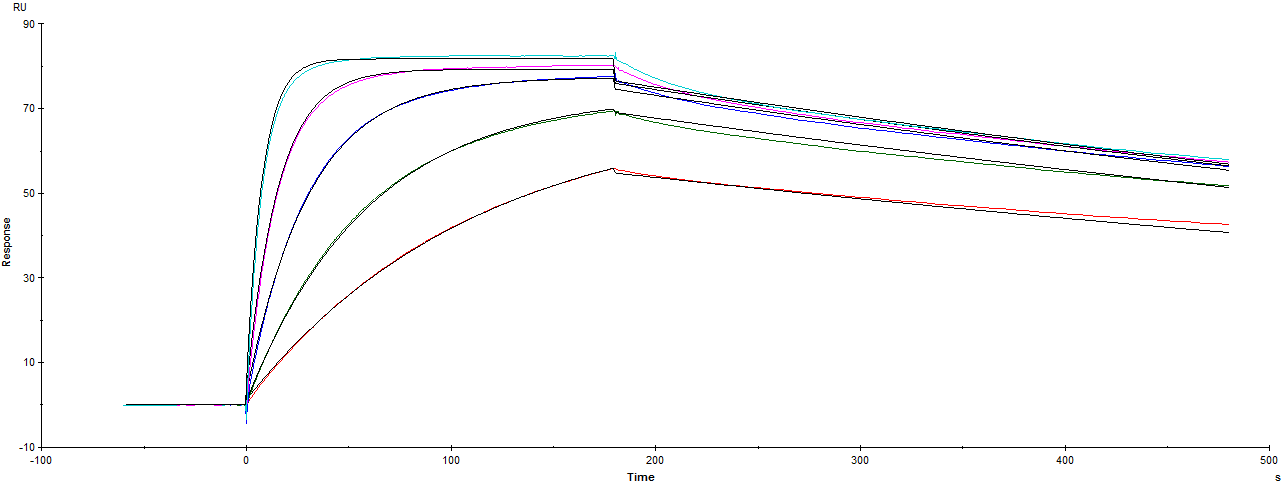
ka(1/Ms)=2.434*E5 kd(1/s)=9.89*E-4 KD(M)=4.064*E-9
SE(Ka)=3.9*E+2 SE(kd)=1.3*E-6
从传感图得知,实验成功监测到信号,信号明显且呈现良好的浓度依赖性。
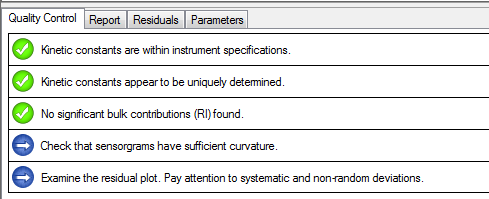
数据QC模块显示数据分析结果合理科学,结果真实可信。
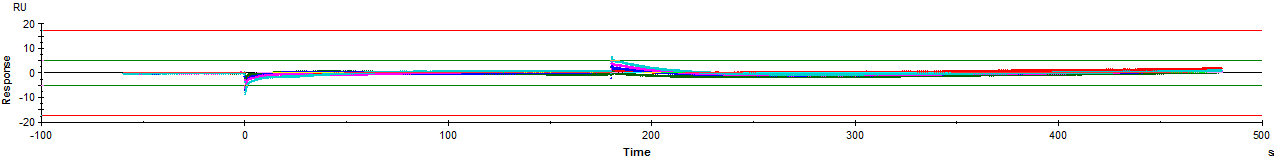
数据Residuals模块表明拟合曲线非常符合实际的数据曲线。
服务联系人:姜丽 0512-62872940 ljiang2007@sinano.ac.cn
10/2020
随着各类新型生物标志物以及药物靶点的发现,尤其是近年来抗体等生物大分子的迅猛发展,引发国内外抗体类治疗药物的研发热潮。抗体药物的生物分析是对药物的有效成分和含量以及药物效价的测定,是批次放行、和稳定性测试以及可比性和特异性研究的重要质控指标。
而抗体药物的分子量其本身复杂的序列、结构,乃至在生产过程中工艺的复杂性,都给分析表征的方法带来诸多困难。而生物学活性贯穿了整个产品的生命周期。从早期靶点的发现、抗体的筛选,再过渡至CMC阶段进行生产、临床应用,到最后上市,都会涉及生物活性的分析。
因此开发出能反映可靠的潜在作用机制,适合QC的生物分析方法,特别是对于新型生物疗法或具有多个活性位点的生物疗法是一件至关重要的事情。

10月24-25日在苏州带来有关于生物分析的 2020 Bioassay Program,Program将关注生物分析方法的生物学功能机制及抗体药物机制、生物分析方法的开发与验证、统计学及方法转移,参会者将在互动气氛中与嘉宾就当前技术、监管观点和法规策略等展开深入互动讨论。本次Program由bioSeedin柏思荟主办,诺唯赞生物协办,中国科学院苏州纳米技术与纳米仿生研究所承办。参与者将有机会获得由诺唯赞生物提供的成长金资助。
Program forBIOASSAY 苏州

嘉宾介绍

徐霆 | 康宁杰瑞创始人、董事长兼CEO
南京大学生物化学学士,中科院生物物理所理学博士、哈佛大学博士后。拥有超过15年的生物创新药研发经验,2008年回国后创立了苏州康宁杰瑞和江苏康宁杰瑞等多家生物制药公司,建立了多个具有自主知识产权的蛋白质和抗体工程技术平台,成功开发20余个生物创新药与30余个生物类似药,申请或授权超过100项专利,建成了符合国际标准的生物大分子产业化基地。
先后在Archemix、Serono和Biogen担任首席研究员和课题负责人等职位。在蛋白质工程和抗体药物筛选、工程化和CMC,以及动物药理、毒理等领域具有丰富的经验和独特的见解。参与开发的多个工程化蛋白质药物已经在欧美上市或处于临床开发阶段。领导康宁杰瑞团队研发的肿瘤免疫新药也将陆续上市。

王媲琳 | 康宁杰瑞非临床部总监
2004年日本爱媛大学学士毕业,2009年获日本京都大学药理学博士学位,之后在日本京都大学药学研究科担任博士后研究员,从事阿尔兹海默病的发病机理研究及创新药物研发,导师为乙酰胆碱酯酶抑制剂多奈哌齐的研发者衫本八郎教授。
2011年加入苏州康宁杰瑞,组建了非临床研究团队,构建了多个治疗领域药物的体内外药效评价体系,主要负责药物成药性评价筛选候选分子,候选分子的作用机理及体内外药效研究、药代动力学及安全性研究等。带领团队开展了多个国家一类新药的非临床研究,目前参与研发的新药项目中已有10个以上在临床开发阶段。

多佳 | 信达生物产品开发活性高级总监
负责生物制药活性及工艺残留方法的开发与验证,对生物分析方法在抗体检测及活性表征领域具有多年工作经验,并参与多项生物制品研发及申报工作。
曾就任于美国百时美施贵宝,对多类生物大分子药物(单抗、双抗和融合蛋白等)的分析方法构建与验证及在不同药品研发与生产阶段(临床前、临床及上市后)的应用有着丰富的经验。

施立明 | 创胜集团分析科学,质量控制及工艺&产品运营副总裁
曾就职于美国基因泰克、安进、礼来、辉瑞等国际知名药企,拥有近22年海外生物制药行业方法研发、质量分析,CMC和团队管理经验。长期专注于生物活性测定方法的开发优化和认证/验证、分析方法转移、分析性能的定量质量控制、偏差/一致性调查、IND/BLA申报。
作为生物药产品开发中的分析负责人,累计参与完成了14个生物创新药和生物类似药的研发及IND/BLA申报,其中8个生物创新药和两个生物类似药实现上市。
参会指南
1.会场地址
2.报名方式:见原文链接
